- Wim Köhler (2004). Gouden genen; Gendoping verlicht blessureleed en
bevordert prestaties.
NRC 14 aug. W&O p. 14,15. Deel artikel zie hieronder. - René Didde en Maarten Evenblij (2003). Eten voor de groei. N&T geb. p. 54 - 60.
Zie beneden. - Huup Dassen (2001). Klierweefsel bevat orgaanspecifieke vaatgroeifactor.
NRC 15 sep. p. 45.
- Marianne Heselmans (2000). Verbod op groeibevorderaars in veehouderij werkt.
2 sep. p.51, k.3-5.
- Sander Voormolen (2000). Transplantatie ooglens geeft
blinde vis weer compleet oog. NRC 29 juli p.33.
k.6-7.
- Blinde vis krijgt oog via lens. Volkskrant 29-7-2000. p.9R. k.6.
Wim Köhler (2004), Gouden genen.
De Olympische Spelen die gisteren van start gingen, zijn waarschijnlijk de laatste zonder gendoping. Gentherapie helpt de zieke mens én de topsporter. Maar de techniek is experimenteel en kan gevaarlijk zijn.
VEEL OLYMPISCHE sporters hebben de afgelopen jaren tijdens langdurige training
jaloers hun oog over een een Belgische dikbilkoe laten gaan.
Die Belgische blauwen, zoals het ras officieel heet, staan zwaar bespierd en
vrijwel vetvrij sloom te herkauwen. Die dieren zijn sterk zonder te trainen.
De atleten vervolgden zwetend hun weg.
De dikbillen hebben een genafwijking waardoor ze - in veeteelttaal - dubbel bespierd zijn. In werkelijkheid bevatten ze 20 procent meer spiermassa, een forser skelet en minder vet. Een ontbrekend stukje DNA in hun myostatine-gen maakt de dieren geliefd bij slagers en liefhebbers van veel en mager vlees. Myostatine is een eiwit dat de spiergroei remt. Bij de dikbillen met genfout werkt het eiwit niet, waardoor de rem op de spiergroei is weggevallen. Muizen, waarbij het gen voor myostatine in het laboratorium is uitgeschakeld, krijgen ook fantastische spieren. Bij mensen werkt het net zo.
Veel sporters dromen van gentherapie (zie kader), van een genetische aanpassing die onoverwinnelijk maakt, of van een genetische ingreep die een slepende blessure wonderbaarlijk snel herstelt. De World Anti Doping Agency (WADA) droomde niet. Gendoping is per 1 januari 2003 verboden. Gevaar voor de gezondheid is één van de twee pijlers onder het verbod van doping in het algemeen. De andere is het ondermijnen van fair play. Beide argumenten gelden onverkort voor gendoping: gentherapie kan gevaarlijk zijn, maar waarschijnlijk ook bijzonder effectief.
Het gendopingverbod van de nieuwe dopingautoriteit WADA is niet absoluut. De
WADA-regels verbieden het 'niet-therapeutische gebruik' van gentherapie.
Die definitie laat ruimte voor discussie,want waar houdt de therapie op en
begint de doping?
Voorbeeld: In de commissie is als hypthetisch geval over Lance Armstrong
gesproken. Armstrong heeft chemotherapie ondergaan
tegen zijn testiskanker. Tegenwoordig is het heel gebruikelijk om tijdens
die chemokuren ook epo te geven, om bloedarmoede te bestrijden. Strikt
noodzakelijk is dat echter niet. Stel dat de gentherapie met epo, die in
ontwikkeling is, toen al had bestaan. En stel dat Armstrong vóór zijn
ziekte een rode-bloedcel-gehalte van 40 had. En dat de gentherapie - waarvan het
effect lang aanhoudt - dat gehalte na zijn ziekte op 45 brengt. Zijn
sportprestaties kunnen daardoor beslist toenemen. Is dat dan therapeutische
of niet-therapeutische gentherapie? Ofwel: is het geoorloofd om er in de
therapie een schepje bovenop te doen om latere sportprestaties te verbeteren?
Blessures
Een atleet hoeft niet eerst kanker te krijgen om van `therapeutische' gentherapie te profiteren. In de orthopedie liggen de voorbeelden voor het opscheppen. Gentherapie-experimenten met een vijftiental verschillende groeifactoren, toegepast bij bot-, pees- en kraakbeenblessures geven in proefdieren inmiddels goede resultaten. Gentherapie met de groeifactor BMP-2 bij konijnen met een gescheurde pees-botaanhechting maakt die verbinding sterker dan hij was (een review over orthopedische gentherapie staat in: The Journal of Gene Medicine (2003) pag 93-108). Hetzelfde staat wellicht te gebeuren na gentherapie bij gescheurde spieren, waarbij een aantal groeifactoren het herstel van spiercellen bewerkstelligen en een andere groeifactor de groei van littekenweefsel tegen gaat.
Gentherapie voor herstel en versteviging van botten, pezen en kraakbeen is niet de enige gendoping die op korte termijn beschikbaar komt. Onderzoekers naar therapieën tegen erfelijke en vaak dodelijke spierziekten experimenteren ook al een aantal jaren met gentherapie. Het zijn therapieën die de afbraak van spieren moeten tegengaan door nieuwe spiercellen te laten groeien. Net als bij de orthopedische gentherapieën gaat het er om om genen voor groeifactoren te introduceren. Myostatine, het eiwit dat een Belgische blauwe tot dikbilkoe maakt is er een voorbeeld van. Het is een remmende factor voor spiergroei, maar eenmaal stil gelegd geeft de therapie hetzelfde effect van een groeibevorderende stof. Een echte spiergroeifactor is IGF-1 (Insuline GroeiFactor 1). Het is min of meer de tegenpool van myostatine. IGF-1 zet de spier aan tot groeien; myostatine zet de rem er op.
Een andere groeifactor waarmee op het ogenblik vergevorderde gentherapie-dierexperimenten bezig zijn is VEGF (Vasculair Endothelium Growth Factor). VEGF stimuleert de groei van nieuwe bloedvaatjes, waardoor spieren beter doorbloed raken en daardoor meer zuurstof en voedingsstoffen uit het bloed kunnen ontvangen. VEGF werkt zowel in de skeletspieren als in het hart. Cardiologen experimenteren met VEGF-gentherapie om verminderde doorbloeding en hartspierschade na een hartaanval en bij hartfalen te herstellen.
En dan is er nog epo (voluit: ErytroPOëtine), de groeifactor die het beenmerg stimuleert tot de aanmaak van zuurstoftransporterende rode bloedcellen. Duursporters presteren beslist beter in de weken na een epokuurtje. Doping met epo is verboden. Tot twee jaar terug vielen wielrenners alleen als epo-gebruiker door de mand als hun gehalte aan rode bloedlichaampjes te hoog was. Bij een hematocrietgehalte boven de 50 mochten wielrenners niet meedoen aan een wedstrijd. Daarna kwam er een urinetest en vervolgens een bloedtest die is gebaseerd op de ouderdomsverdeling van de rode bloedcellen. Rode bloedcellen worden op zijn hoogst een paar maanden oud en rijpen en sterven in een bepaald tempo. Zijn er opeens veel rode bloedcellen van een een bepaalde leeftijd, dan is duidelijk dat er is ingegrepen om extra rode bloedcellen te groeien.
Gentherapie met epo is mogelijk door een kopie van het epo-gen in te bouwen in uit het bloed geďsoleerde lichaamscellen van de sporter. En die epo-producerende cellen terug te spuiten in het lichaam van de atleet. Dat levert een verhoogde epo-productie en als die productie aanhoudt is na enige weken in de leeftijdverdeling van rode bloedcellen niet meer te zien of er epo wordt gebruikt. Gentherapie met het epo-gen wordt ontwikkeld omdat veel nierpatiënten jarenlang epo spuiten. Zij zouden met gentherapie veel langduriger geholpen zijn.
Sporters met een erfelijk verhoogd epo-gehalte zijn voorlopig de enigen die vrijuit profiteren van hun vele rode bloedcellen. In iedere duursport zijn er een paar atleten die mogen deelnemen ondanks hun hoge hematocrietgehalte. Het vaak aangehaalde voorbeeld is Eero Mäntyranta, een Finse langlaufskiër die in 1964 twee gouden medailles won op de Olympische winterspelen. Hij kwam uit een familie van berucht goede duursporters.
één dode
Gentherapie verkeert nog in het experimentele stadium. Nog maar een paar duizend mensen hebben gentherapie ondergaan. Een handjevol mensen met een zeldzame ziekte van het afweersysteem zijn beter geworden door gentherapie. Maar ook is er een mens bij een gentherapie-experiment overleden (door een te hoge dosis) en twee kinderen kregen leukemie na een (overigens voor hun immuunziekte succesvolle) gentherapie. Succesvolle gentherapie-experimenten met het epo-gen kregen een zware terugslag nadat begin dit jaar bekend werd dat sommige proefdier-aapjes aanvankelijk epo produceerden en veel rode bloedcellen kregen, maar uiteindelijk door een afweerreactie ernstige bloedarmoede kregen. De bijwerkingen traden bij enkele proefdieren op. Niet bij allemaal.
Gendoping is niet alleen aantrekkelijk omdat er waarschijnlijk echte prestatieverhoging mee mogelijk is. Deskundigen breken zich op het ogenblik het hoofd over de vraag hoe gendoping opgespoord kan worden. Als je accepteert dat je geen stukje spier kunt weghalen bij een sporter die op het punt staat aan een wedstrijd deel te nemen, dan is eigenlijk de enige mogelijkheid om van iedere atleet regelmatig een eiwitprofiel te maken. De proteonomics maken het mogelijk om in één klap de hoeveelheid van honderden of duizenden eiwitten in het bloed te bepalen. Je moet dan vaststellen hoe de eiwitsamenstelling verschuift na gentherapie met epo, of IGF-1 of een andere groeifactor. Inderdaad, dopingcontrole was al ingewikkeld, maar op deze manier wordt het helemaal hightech.
De komende jaren zullen nog veel meer genen opduiken die van invloed zijn op sportprestaties en - meer in het algemeen - fitness. Een internationale groep fysiologen en sportgeneeskundigen heeft inmiddels al een Human Gene Map for Performance and Health-Related Fitness Phenotypes opgesteld. Daar staan 90 genen uit het gewone genoom en 14 genen uit de mitochondriën (de energieleverende celcompartimenten met eigen DNA) op. Het myostatine-gen staat (onder zijn oude naam GDF8) ook op hun lijst.
vader
Dat myostatine ook bij mensen werkt is duidelijk omdat mensen die te veel myostatine in hun bloed hebben last krijgen van spierzwakte. Voor sporters is belangrijk dat een tekort aan myostatine de spiergroei bevordert. Dat blijkt uit de enkele weken geleden wereldkundig geworden geschiedenis van een vierjarig Duits jongetje. Het kind is het zoontje van een voormalig professionele, goedbespierde atlete en een in medische kringen onbekend gebleven vader. Bij zijn ongecompliceerde geboorte (veel dikbilkoeien kunnen alleen met een keizersnede bevallen) was het jongetje al flink gespierd. De spierontwikkeling ging door en toen hij vierenhalf was kon hij 3 kilo zware halters met gestrekte armen vasthouden. Genanalyse van moeder en zoontje (DNA van andere familieleden was niet beschikbaar) bracht een genafwijking aan het licht waardoor myostatine niet ontstaat. De moeder heeft de genafwijking in één van haar beide myostatinegenen en profiteerde er tijdens haar sportcarričre van, gezien haar spierontwikkeling. Het zoontje heeft de afwijking in beide genen. Dat roept de vraag op wie nu eigenlijk die onbekend gebleven vader is. Een collega-sporter die zijn successen ook dankte aan die genafwijking? Komt die genafwijking vaker voor bij sporters? De Duitse onderzoekers zochten naar de genafwijking bij 200 controlepersonen, maar vonden hem niet. Het is dus geen normale genetische variant, concluderen ze. Maar interessant was geweest als ze ook het DNA van 200 topgewichtheffers en kogelstoters hadden bekeken.
De opa en overgrootvader van het jongetje stonden als zeer sterke mannen bekend. Opa was stratenmaker die de trottoirbanden zonder takel van de vrachtwagen tilde. Duitse artsen beschreven het onderzoek naar het myostatinegen van het jongetje deze zomer in The New England Journal of Medicine (24 juni) en ze concluderen dat het er op lijkt dat ook in mensen 'spiermassa en -sterkte therapeutisch kunnen worden verbeterd door stilleggen van myostatine in patiënten met spierziekten.
Niet alleen onderzoekers die medicijnen zoeken tegen de - vaak op jonge leeftijd
dodelijke - spierziekten als spierdystrofie zijn in myostatine geďnteresseerd.
Veel wetenschappelijke publicaties komen uit de hoek van het veeteeltonderzoek.
De kennis over de werking van myostatine bij koe, rat, muis, kip en kalkoen
komt van onderzoekers als dr. Se-Jin Lee van Johns Hopkins University in
Baltimore die op zoek ging naar 'mogelijke myostatine remmende moleculen
die toegepast kunnen worden ter bevordering van spiergroei'.
Lee ontdekte de werking van myostatine. Hij deponeerde de naam en schrijft
nu Myostatin. Lee baseerde zijn bedrijf MetaMorphix op myostatine. Op
MetaMorphix' website heet myostatine 'beredeneerbaar de belangrijkste
ontdekking in de geschiedenis van de veeteelt'.
De werking van myostatine is evolutionair goed geconserveerd. In koeien, varkens,
kippen, kalkoenen
en mensen werkt het eiwit op dezelfde manier. Een genetisch gemanipuleerde
varkenssoort waarin het myostatinegen is uitgeschakeld (zoals door een
natuurlijke mutatie in de Belgische dikbillen en de Duitse familie gebeurde)
is dus bijna een garantie voor een vleesrijk en wat vetvrijer varken.
Voor het blokkeren van myostatine is strikt genomen niet eens gentherapie nodig. Follistatine is een lichaamseigen middel dat myostatine blokkeert. Het middel komt wel uit het genetisch onderzoek voort. Voor begerige sporters: een korte zoektocht op internet is voldoende om Amerikaanse leveranciers voor follistatine te vinden. Het spul is alleen te koop voor biochemisch onderzoek. Het is niet gezuiverd om bij mensen te worden ingespoten.
KADER: EEN SPUITJE MET GENEN
Gentherapie is een medische behandeling die één of meerdere genen in
lichaamscellen van een patiënt plaatst, met de bedoeling de werking van een
ontbrekend of tekortschietend gen over te nemen.
Een gen bestaat uit een langgerekt DNA-molecuul met de code voor een
lichaamseiwit. Dat eiwit kan een bouwsteen voor een cel zijn, of een enzym
dat een biochemische reactie katalyseert, of een eiwit met een
boodschapperfunctie, zoals de groeifactoren die bij gendoping een grote rol
spelen. Groeifactoren stimuleren (of remmen) meestal de celdeling in bepaalde
weefsels.
Gentherapie is alleen effectief als het therapeutische gen in de celkern
terecht komt en onderdeel wordt van het systeem dat de eiwitsynthese in een
cel regelt. De eenvoudigste gentherapie bestaat uit het inspuiten (
bijvoorbeeld in een spier) van kaal DNA. Dat is eenvoudig. Maar de kans dat
het DNA dan ooit in een celkern actief wordt is niet groot.
Effectiever is het om het gen onder te brengen in een virus dat menselijke
cellen kan infecteren. Virussen zijn er van nature in gespecialiseerd om hun
genen in de celkern van de geďnfecteerde cel 'aan het werk' te zetten.
Gentherapievirussen zijn zo veranderd dat ze geen ziekte veroorzaken en zich
niet meer kunnen vermenigvuldigen.
Een probleem bij gentherapie is om het therapeutische gen terecht te laten
komen in de cellen waar het aan het werk moet. En niet in andere. Sommige
virussen hebben een voorkeur voor bijvoorbeeld spiercellen en daar kan bij
gentherapie gebruik van worden gemaakt. Een andere mogelijkheid is om cellen
bij de patiënt weg te nemen, de virale gentherapie in het lab uit te voeren,
en de veranderde cellen weer bij de patiënt te implanteren. Dat is vaak
mogelijk bij gentherapie voor kraakbeen-, pees- en botblessures.
Het inbrengen van een gen heeft eigenlijk alleen zin als de synthese van
het eiwit waar het gen voor codeert, gereguleerd wordt. Anders bestaat het
gevaar dat er te veel of te weinig eiwit ontstaat. Daarom krijgt een gen veelal
een regulerende DNA-sequentie mee die reageert op boodschappermoleculen in
de cel die tot eiwitsynthese aanzetten. Ook zijn er tegenwoordig
gentherapiesystemen in ontwikkeling die pas actief worden als de patiënt
een bepaald `medicijn' slikt.
 |
| Dikbilkoeien zijn extra gespierd door een genafwijking in hun mysotatinegen. Het ontbreekt hen daardoor aan myostatine, een natuurlijke rem op spiergroei. |
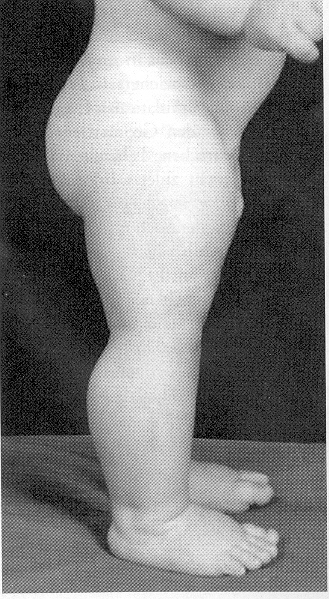 |
| Een fout myostatinegen maakt ook mensen sterk bespierd. Dat is te zien aan de kuiten en dijbenen van een zeven maanden oud staand (!) Duits jongetje. Hij heeft geen myostatine in zijn bloed. Zijn moeder maakte weinig myostatine en was een professioneel atlete. |
Het zou interessant zijn om krachtsporters te onderzoeken op myostatinetekort.
René Didde en Maarten Evenblij (2003). Eten voor de groei.
N&T geb. p. 54 - 60.
Lengte van volwassen mannen:
Periode nC. Gem. Lengte cm Van wie? 50 - 250 176 10 Valkenburgers 450 - 750 174 7 man uit Oosterbeinum 800 - 1100 172,5 13 Susterense monniken 1100 - 1500 173,5 23 Maastrichtse kannuniken 1250 - 1450 170,5 25 Delftenaren 1250 - 1600 170,5 80 Dordrechters 1450 - 1550 169 19 Delftenaren 1450 - 1550 169,5 11 man uit Gorinchem 1600 - 1850 171,5 19 man uit Breda 1650 - 1800 166 41 walvisjagers op Spitsbergen 1650 - 1800 166,5 102 Leidenaren 1750 - 1850 173 31 Zwollenaren 1750 - 1850 169,5 70 man uit Alkmaar 1820 169 382 militiesoldaten uit 7 steden 1850 169,5 82 man uit Den Bosch 1870 167,5 722 militiesoldaten uit 7 steden 1870 - 1920 166 86 Leidenaren 1950 176 1213 inwoners uit heel Nederland 1960 178 391 inwoners uit heel Nederland 1980 182 3233 inwoners uit heel Nederland 2000 184 900 inwoners uit heel NederlandDe Nederlandse man groeit nu 1,3 mm per jaar. In 2003 is de gem. lengte 1,849 m voor de mannen en 1,712 m voor de vrouwen.