4H-1.8 Osmose bij planten.
Als je bedenkt dat plantencellen hun water uit de bodem halen kun
je ook bedenken dat het water celwanden moet passeren en dat die
celwanden nat van het bodemwater moeten zijn; bodemwater met daarin
opgeloste stoffen.
Celwanden zijn goed te vergelijken met een
papieren zakdoekje, een tissue, een vlechtwerk van cellulose
(= celstof). Binnen dat zakdoekje zit dan de celmembraan, vervolgens een
dun laagje cytoplasma en dan weer de vacuolemembraan die de
vacuole omgeeft. Je mag het celmembraan samen met het cytoplasma
en vacuolemembraan zien als één enkele semipermeabele membraan.
De vacuole is gevuld met water met daarin opgeloste stoffen(*).
* In het vacuolewater of -vocht is de concentratie aan
opgeloste deeltjes beduidend groter dan de concentratie deeltjes
in het celwand- of bodemwater.
Neem voor jezelf als richtlijn dat bij vers plantenmateriaal
de concentratie aan opgeloste deeltjes in de vacuole 10x groter
is dan in de celwand. Bijvoorbeeld in de celwand is de concentratie
1 % en in de vacuole 10 %. Neem gewoon makkelijke getallen.
Onder deeltjes versta je te grote moleculen en ionen (geladen
deeltjes) die niet spontaan door middel van diffusie door de
semipermeabele membraan kunnen. Water-, zuurstof- en
koolstofdioxide-moleculen zijn voldoende klein en niet geladen
zodat ze wel door de semipermeabele membraan kunnen diffunderen.
* Als we bovengenoemde getallen aannemen dan zit er in de
celwand 99 % water en 1 % opgeloste deeltje,
in de vacuole zit dan 90 % water en 10 % opgeloste deeltjes.
Ik herhaal het nog een keer: In de celwand zit 99 % water en in
de vacuole zit maar 90 % water.
Omdat water wel door diffusie door de semipermeabele laag
(= celmembraan, cytoplasma en vacuolemembraan) kan is er dus een
grotere aandrang van water vanuit de celwand naar vacuole
dan omgekeerd. Het Griekse woord voor 'aandrang', het aan- of
indringen van het water, is osmose.
* We vergelijken de cel met een autoband. Stel dat we de
ruimte in de autoband (vgl. vacuole) zouden oppompen met water,
dan wordt de binnenband (vgl semipermeabele membraan) tegen de
buitenband (vgl. celwand) geduwd. Op een gegeven moment duwt de
buitenband (celwand) met een even grote kracht terug als de kracht
waarmee het (vacuole)water de binnenband (semipermeabele membraan)
tegen de buitenband (celwand) duwt.
Zie afbeelding 70 in je boek. In de lichtgroen gekleurde celwand
zit 99 % water. In de witte vacuole zit maar 90 % water. Er wil
meer water naar binnen dan eruit, er is sprake van een osmotische
druk richting vacuole. De vacuole zwelt enigszins en duwt het
cytoplasma tegen de celwand. De celwand duwt op een gegeven moment
even sterk terug. Er heerst dan een bepaalde (evenwichts)druk die
we turgor noemen.(Grieks: turgor
'zwellingsdruk';
turgere 'zwellen')
Plantencellen in vers materiaal zorgen er steeds voor dat in de
vacuole meer opgeloste deeltjes voorkomen dan in de celwand, dus,
met andere woorden, plantencellen zorgen ervoor dat in de celwand altijd
een hogere waterconcentratie heerst dan in de vacuole. Daardoor is
er altijd een osmotische druk naar binnen toe die evenwicht maakt
met de celwand-tegendruk. De inwendige druk noemen we turgor
en cellen met turgor noemen we turgescent.
Als je verse sla bereidt met een dressing erop dan dringt de
dressing in de celwanden. Het gevolg zal zijn dat water in de
celwanden wordt verdrongen door de dressing. Stel dat de
waterconcentratie in de celwanden 85 % wordt, terwijl deze in de
vacuolen nog 90 % is. De osmotische druk is dan naar buiten gericht,
de vacuolen lopen deels leeg en je ziet de sla slinken.
* We trekken de vergelijking met de met water gevulde
autoband (cel) nog even door. Als de band (cel) meer en meer
leegloopt zal de druk in de band (turgor) minder en minder worden.
Op een gegeven moment duwt de lucht (water) de binnenband (semipermeabele
wand = celmembraan + cytoplasma + vacuolemembraan) niet meer tegen
de buitenband, de druk (turgor) is dan nul geworden. Loopt er nog
meer water uit dan laat de binnenband los van de buitenband (het
(cyto)plasma laat los
(lyse) van de celwand =
plasmolyse). De druk (turgor) blijft
uiteraard nul.
Opvallend is dat de stugge buitenband (celwand) wel op zichzelf
blijft staan. De band (cel) is wat minder dik geworden, maar je
ziet aan de buitenkant niet dat de binnenband (membranen + plasma)
los erin ligt. Dat zie je wel als je in de band kijkt (in de cel
kijkt met een microscoop).
De situatie waarbij de turgor net nul gaat worden, dus de
celmembraan net wel net niet loslaat van de celwand noemen we
grensplasmolyse.
* Als we weer aan onze slabladen denken, waarbij water uit
de vacuolen naar de celwanden, met daarin de dressing, loopt, dan
kunnen we ons voorstellen hoe de concentratie in de vauoles toe
gaat nemen. De achtergebleven deeltjes komen immers steeds dichter
op elkaar te zitten. De deeltjes komen 'samen'
(con-) dichter in
het 'centrum' te zitten, de
'concentratie' wordt
groter. Als die concentratie 15 % is geworden ofwel als de
waterconcentratie in de vacuole 85 % is geworden, dus net zo groot als
in de celwand, dan is de aandrangsdruk, de osmotische druk weg.
Het leeglopen stopt. Het hangt er maar vanaf of de celmembraan nog wel
een beetje of in het geheel niet meer tegen de celwand duwt, dus of
er nog wel iets of geen turgor meer is.
* Het verschil tussen osmotische
waarde en
osmotische druk.
Als we het celwandwater of bodemwater (1 % deeltjes of 99 % water)
uit ons voorbeeld in de osmometerbak hadden gedaan en het
vacuolevocht (10 % deeltjes of 90 % water) in de osmometerbuis dan
hadden we de vloeisof in de osmometerbuis een aantal meters zien
stijgen boven het niveau van de bak.
Stel dat die 9 % concentratieverschil goed is voor 18 m stijging,
dus 2 m stijging per procent verschil, dan is de osmotische
druk
180 kPa.
(Bij een autoband betekent 180 kPa nagenoeg hetzelfde
als 1,8 atmosfeer of 1,8 bar.)
Onthoudt:
Voor de leerlingen met veel natuurkundige interesse zal ik dit
apart uitleggen. De eenheid van druk is de Pa (pascal = N/m2).
1 kPa (kiloPascal) = 1000 Pa.
Stel dat in de celwand (en dus in de osmometerbak) een oplossing had
gezeten met 2 % deeltjes en in de vacuole (dus in de osmometer) een
11 % oplossing. Het verschil is dan weer 9 % aan deeltjesconcentratie
of aan waterconcentratie en de stijging zal weer 18 m zijn ofwel de
aandrangsdruk, de osmotische druk is
andermaal 180 kPa.
Ik denk dat jullie, samen met mij, nu wel het idee zullen 'bekomen' om
tabelletjes aan te leggen voor allerlei oplossingen met verschillende
concentratie. OK. We doen in de buitenbak van de osmometer steeds
zuiver water (0 % deeltjes = 100 % water) en in de osmometerbuis een
oplossing met steeds sterkere concentratie, 1 %, 2 % etc. We vinden
dan stijgingen van 2 m, 4 m etc, respectievelijk osmotische drukken
van 20 kPa, 40 kPa etc. Echter we noemen nu deze osmotische drukken, die
zijn gemeten ten opzichte van zuiver water,
osmotische
waarden.
Het gemak is nu dat je geen osmometer meer nodig hebt, maar alleen
de tabel. Zit in de buitenbak 3,45 % (osmotische
waarde
69 kPa) en in de buis 18 % (osmotische waarde
360 kPa), dan weten
we dat de osmotische druk zal zijn
360 kPa - 69 kPa = 291 kPa.
N.B.: Tot nu toe heb ik gewerkt met gemakkelijke getallen, namelijk dat 1%
overeenkomt met 20 kPa, maar de echte
getallen staan in
ons BINAS-boekje en dat is tabel
77 op blz. 146 en 147.
Nog een 'vreemd' voorbeeldje: De osmometerbak vullen we met
0,5 % onvervuild zeewater en de osmometerbuis met menselijk
bloedplasma. Hoe hoog is dan de osmotische druk ofwel hoe hoog
stijgt de vloeistof in de meter?
Oplossing: Tabel 77 in ons BINAS-boekje vertelt ons dat een 0,5 %
zeewateroplossing een osmotische waarde heeft van
0,35 . 106 Pa = 350 kPa en bloedplasma heeft een
gemiddelde osmotische waarde van 740 kPa.
Dit verschil levert een osmotische druk van
740 - 350 = 390 kPa.
De vloeistofkolom in de osmometerstijgbuis zal dan een hoogte
bereiken van 39 m.
Kerktorenhoog? Veel hč!
(Voor de geďnteresseerden zal ik uitleggen dat we
dat niet meer met 'flathoge of kerkhoge buisjes' meten.)
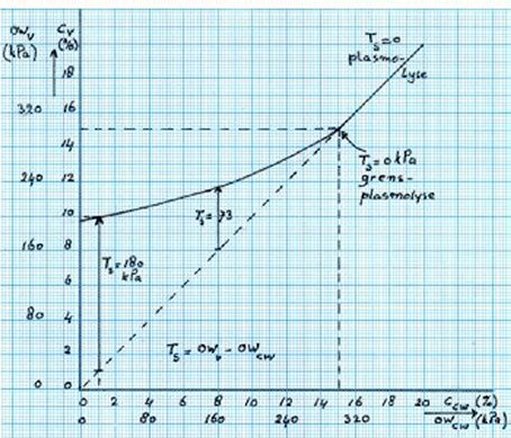
Hiernaast heb ik een diagram getekend dat in grote lijnen hetzelfde is als het diagram in ons leerboek. Erbij zijn nu getallen gezet die overeenkomen met onze vuistregel die hierboven al is genoemd, nl. als een verse cel in haar celwandwater een deeltjesconcentratie heeft van 1 % dan tracht deze cel er in de vacuole 10 % van te maken.
Horizontaal in het diagram staat de concentratie in het celwandwater Ccw in % en parallel daarmee de osmotische waarde van dat (bodem)water in die celwand OWcw in kPa. Let wel dat het willekeurig gekozen getallen zijn omdat we niet weten wat voor soort deeltjes er precies in de celwand (en vacuole) voorkomen.
Verticaal staat de vacuoleconcentratie Cv in % samen met de osmotische waarde van dat vacuolevocht OWv in kPa.
Onder dit diagram had ik eigenlijk de tekeningen van een cel moeten
weergeven. Leg het boek er maar naast en kijk daar in! Je ziet dan
dat als je naar links
van 'p' gaat (ik heb daarvoor 15 % (300 kPa) genomen), je een meer
en meer zwellende cel ziet met een toenemende turgor. Rechts van 'p' zie je
een cel met een steeds toenemende plasmolyse, waarbij de celwand de
grootte van de cel bepaalt.
De turgor wordt weergegeven met Ts. De 's' in Ts staat
voor stationair en daar wordt mee bedoeld dat na een, eventueel
opzettelijke, verandering van de osmotische waarden er weer een
evenwichtssituatie is ingetreden. De turgor wordt weergegeven door
de formule
In feite hebben we de formule hiervoor al gebruikt, nl. voor een
cel uit vers weefsel met 1 % conc. in de celwand en 10 % conc. in
de vacuole. De turgor Ts = 200 - 20 = 180 kPa. De
formule hadden we al toegepast en toen gelukkig door 'gewoon logisch na
te denken'.
Leggen we de cel in zuiver water (0 %), dan wordt de osmotische
druk naar binnen toe een stukje groter. De vacuole zwelt een
fractie op, maar daardoor zakt de concentratie in de vauole a
little bit en wordt bijv. 9,7 %.
De turgor is nu 194 - 0 = 194 kPa geworden. Geen wonder iets
water is erbij ingeperst, de cel is nog een beetje meer gezwollen,
meer turgescent.
Hadden we de cel in een oplossing van 8 % gelegd dan was de
osmotische druk van 180 kPa (10 % - 1 %) plots gezakt naar
10 % - 8 % = 2 % ofwel 40 kPa.
De celwand (vgl. de buitenband) veert nog terug met een druk van
180 kPa en die zorgt ervoor dat een beetje water de vacuole uit
wordt geperst. Daardoor stijgt de concentratie in de vacuole en
wel tot een hoogt van 11,65 %. Een nieuwe stationaire situatie
heeft zich dan ingesteld.
De nieuwe, nu lagere turgor, is dan 11,65 % - 8 % ofwel
233 - 160 = 73 kPa.